La desinfección tiene por objeto eliminar a los microorganismos patógenos y garantizar la ausencia de todo germen infeccioso (bacteria o virus) en las aguas. Los productos clorados son las sustancias utilizadas con mayor frecuencia en el tratamiento químico del agua gracias a su inocuidad y facilidad para el control de sus niveles. Todos los productos clorados utilizados en el tratamiento producen ácido hipocloroso (HClO) al reaccionar con el agua. El ácido hipocloroso es un ácido débil que se disocia a hipoclorito (ClO-) en el agua según un equilibrio condicionado por el valor del pH. La suma de estas 2 formas constituye lo que se llama el cloro libre. En las aguas con un pH alto, la mayor parte del ácido hipocloroso (cloro activo) se convierte en ión hipoclorito (cloro potencial), una forma de cloro con muy bajo poder desinfectante. El cloro combinado es el resultado de la combinación del cloro con el amoniaco y materia orgánica nitrogenada que contiene el agua. La suma del cloro libre y el cloro combinado constituye el cloro total.
CLORO LIBRE + CLORO COMBINADO = CLORO TOTAL
Aunque no se hayan observado efectos adversos en humanos expuestos a la desinfección por cloro las distintas legislaciones establecen valores paramétricos para la presencia de cloro en las distintas aguas. En el agua de consumo humano el RD 140/ 2003, de 7 de febrero, por el que se establecen los criterios sanitarios de la calidad del agua de consumo humano, indica un valor máximo paramétrico de 1 mg/L (en la red de distribución) para el cloro libre en el anexo I. Por otro lado el RD 742/2013, de 27 de septiembre, por el que se establecen los criterios técnico-sanitarios de las piscinas, indica un valor paramétrico entre 0,5 y 2,0 mg/L para el cloro libre en el anexo I. Química del cloro y cloraminas Tal y como hemos indicado anteriormente todos los productos clorados utilizados en el tratamiento producen ácido hipocloroso (HClO) al reaccionar con el agua. Este ácido débil se disocia en el agua según el equilibrio: 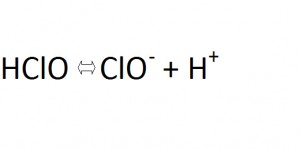 La suma de estas dos formas (HClO y ClO-) constituye lo que se llama el cloro libre y el equilibrio pone de manifiesto que su ámbito de existencia depende del pH, como se muestra en el siguiente gráfico. Para un pH entre 6 y 9, el procentaje de ácido hipocloroso disminuye rápidamente a favor del ión hipoclorito.
La suma de estas dos formas (HClO y ClO-) constituye lo que se llama el cloro libre y el equilibrio pone de manifiesto que su ámbito de existencia depende del pH, como se muestra en el siguiente gráfico. Para un pH entre 6 y 9, el procentaje de ácido hipocloroso disminuye rápidamente a favor del ión hipoclorito. 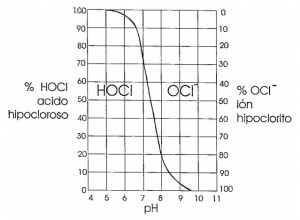 El cloro reacciona con numerosos compuestos minerales (hierro, nitrógeno amoniacal, nitritos, cianuros….), así como con la materia orgánica de las aguas (sustancias húmicas en particular). Reacciones cloro/amoníaco La acción del cloro sobre el nitrógeno amoniacal presenta un interés particular, esta reacción produce en primer lugar la formación de monocloraminas (NH2Cl) y en segundo lugar la de di- y tricloraminas (NHCl2 y NCl3). El conjunto de las cloraminas de procedencia mineral así como las cloraminas orgánicas constituyen el cloro combinado que junto al cloro libre constituyen el cloro total. Método de determinación de cloro Existen distintos métodos de determinación con diferencias en la especificidad, sensibilidad y reproducibilidad. El método de la dietil-p-fenilenodiamina (DPD) sin embargo es el más extendido debido a su rapidez de aplicación, reproducibilidad y sensibilidad, permitiendo la determinación del cloro libre y total, pudiéndose desarrollar por espectrometría o por volumetría. El DPD se oxida en presencia de distintos oxidantes, incluyendo el cloro que reacciona instantáneamente con el DPD. La determinación del cloro total requiere la adición de iones yoduro. En presencia de yoduro las cloraminas liberan yodo que oxidan la DPD, lo que permite su determinación en condiciones bien definidas. La aplicación de las determinaciones con la DPD requiere controlar l¡bien las condiciones de pH recomendadas (6,2<pH<6,5). Un pH demasiado bajo ocasionaría la reacción de las monocloraminas al mismo tiempo y además puede aparecer una cloración por el oxígeno disuelto por el pH bajo. La diferencia entre el cloro total (en presencia de yoduros) y el cloro libre nos da el valor del cloro combinado, siendo el rango de aplicación de este método de 0 a 5 mg/L de cloro, por lo que es un método idóneo para la determinación de cloro tanto en agua potable como en agua de piscinas. Reactivos DPD (DPD1, DPD3 y DPD4) Los reactivos comerciales son conocidos como DPD1, DPD3 y DPD4 a continuación se indica a que reactivo hace referencia cada una de estas denominaciones. El DPD1 es el reactivo DPD utilizado en la determinación de cloro libre, es decir el reactivo dietil-p-fenilenodiamina (DPD) en sí estabilizado a un pH correcto mediante tampón para la medida. El DPD3 es el reactivo yoduro potásico que al adicionarlo a la muestra en presencia de cloraminas genera yodo que oxida el DPD y permite la medición del cloro combinado junto con el libre, lo que llamamos CLORO TOTAL. El reactivo DPD4 sería el utilizado para la determinación de cloro total. En el caso del reactivo líquido sería DPD1+DPD3, en polvo viene todo incluido en el mismo sobre siendo directamente DPD4. Método DPD para otros oxidantes El método DPD no es selectivo para el cloro y por ello para la determinación de otros oxidantes (como por ejemplo ozono, bromo o dióxido de cloro) también se utiliza este método. En los casos en que se encuentran el cloro junto con otro de los oxidantes nombrados en la misma muestra, hay procedimientos para la determinación por separado de los mismos.
El cloro reacciona con numerosos compuestos minerales (hierro, nitrógeno amoniacal, nitritos, cianuros….), así como con la materia orgánica de las aguas (sustancias húmicas en particular). Reacciones cloro/amoníaco La acción del cloro sobre el nitrógeno amoniacal presenta un interés particular, esta reacción produce en primer lugar la formación de monocloraminas (NH2Cl) y en segundo lugar la de di- y tricloraminas (NHCl2 y NCl3). El conjunto de las cloraminas de procedencia mineral así como las cloraminas orgánicas constituyen el cloro combinado que junto al cloro libre constituyen el cloro total. Método de determinación de cloro Existen distintos métodos de determinación con diferencias en la especificidad, sensibilidad y reproducibilidad. El método de la dietil-p-fenilenodiamina (DPD) sin embargo es el más extendido debido a su rapidez de aplicación, reproducibilidad y sensibilidad, permitiendo la determinación del cloro libre y total, pudiéndose desarrollar por espectrometría o por volumetría. El DPD se oxida en presencia de distintos oxidantes, incluyendo el cloro que reacciona instantáneamente con el DPD. La determinación del cloro total requiere la adición de iones yoduro. En presencia de yoduro las cloraminas liberan yodo que oxidan la DPD, lo que permite su determinación en condiciones bien definidas. La aplicación de las determinaciones con la DPD requiere controlar l¡bien las condiciones de pH recomendadas (6,2<pH<6,5). Un pH demasiado bajo ocasionaría la reacción de las monocloraminas al mismo tiempo y además puede aparecer una cloración por el oxígeno disuelto por el pH bajo. La diferencia entre el cloro total (en presencia de yoduros) y el cloro libre nos da el valor del cloro combinado, siendo el rango de aplicación de este método de 0 a 5 mg/L de cloro, por lo que es un método idóneo para la determinación de cloro tanto en agua potable como en agua de piscinas. Reactivos DPD (DPD1, DPD3 y DPD4) Los reactivos comerciales son conocidos como DPD1, DPD3 y DPD4 a continuación se indica a que reactivo hace referencia cada una de estas denominaciones. El DPD1 es el reactivo DPD utilizado en la determinación de cloro libre, es decir el reactivo dietil-p-fenilenodiamina (DPD) en sí estabilizado a un pH correcto mediante tampón para la medida. El DPD3 es el reactivo yoduro potásico que al adicionarlo a la muestra en presencia de cloraminas genera yodo que oxida el DPD y permite la medición del cloro combinado junto con el libre, lo que llamamos CLORO TOTAL. El reactivo DPD4 sería el utilizado para la determinación de cloro total. En el caso del reactivo líquido sería DPD1+DPD3, en polvo viene todo incluido en el mismo sobre siendo directamente DPD4. Método DPD para otros oxidantes El método DPD no es selectivo para el cloro y por ello para la determinación de otros oxidantes (como por ejemplo ozono, bromo o dióxido de cloro) también se utiliza este método. En los casos en que se encuentran el cloro junto con otro de los oxidantes nombrados en la misma muestra, hay procedimientos para la determinación por separado de los mismos.
DETERMINACIÓN DE BROMO EN PRESENCIA DE CLORO
Al realizar la determinación mediante DPD de muestras con contenido de cloro y bromo utilizando reactivo DPD1 el resultado obtenido será la suma de ambas especies. La adición de glicina antes de determinar el cloro libre transforma el cloro libre en formas no reactivas y el bromo queda como forma reactiva. En caso de que la determinación se realice con un fotómetro de cloro, la concentración de bromo se expresará como mg/L Cl2, para calcular los mg/L Br2 se multiplicará por 2.25 el valor obtenido. Relación entre masa molar molecular del Bromo/Cloro = 159.8/70.90 = 2.25 Sin embargo tanto HANNA al igual que las indicaciones del “Análisis de Aguas” de Jean Rodier la determinación del contenido de Bromo mediante método DPD se realiza según método descrito para el cloro total, por lo tanto con reactivo DPD4.
DETERMINACIÓN DE DIÓXIDO DE CLORO EN PRESENCIA DE CLORO
Al realizar la determinación mediante DPD de muestras con contenido de cloro y dióxido de cloro utilizando reactivo DPD1 el resultado obtenido será la suma de ambas especies. La adición de glicina antes de determinar el cloro libre transforma el cloro libre en formas no reactivas y el dióxido de cloro queda como forma reactiva. En caso de que la determinación se realice con un fotómetro de cloro, la concentración de dióxido de cloro se expresará como mg/L Cl2, para calcular los mg/L ClO2 se multiplicará por 1.9 el valor obtenido. A diferencia que en el caso del Bromo y Ozono donde la relación para el cálculo del factor de conversión es la relación directa entre las masas molares moleculares de las especies, el caso del dióxido de cloro la relación se calcula como masa molar dióxido de cloro/cloro equivalente (lo que representa 67.44/35.45=1.9)
DETERMINACIÓN DE OZONO EN PRESENCIA DE CLORO
La determinación del ozono por método DPD se realiza siguiendo el procedimiento de determinación de cloro total utilizando reactivo DPD4, por lo que el resultado será la suma del ozono y cloro total de la muestra. La adición de glicina a la muestra enmascara el ozono quedando el cloro total como especie reactiva. El cálculo del ozono se realiza mediante resta del resultado sin adición de glicina y tras la adición de glicina. La resta indicará la concentración de ozono expresada como mg/L Cl2, para calcular los mg/L O3 se multiplicará por 0.67 el valor obtenido. Relación entre masa molar molecular del Ozono/Cloro = 48/70.90 = 0.67 Fuentes: https://www.msssi.gob.es/ciudadanos/saludAmbLaboral/agenBiologicos/pdfs/2_leg.pdf Jean Rodier, Bernard Legube, Nicole Merlet y colaboradores, “Análisis del agua” ACCEDE A LA INSTRUMENTACIÓN DE MEDIDA: FOTOMETRÍA PARA AGUAS POTABLES Y FOTOMETRÍA PARA PISCINAS










Síguenos